amidas
[ad_1]
Generalidades e propriedades das amidas.
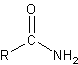
a amidas São compostos derivados de ácidos carboxílicos e possuem a seguinte estrutura geral:
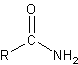
O que acabamos de descrever é um amida primária, mas eles também existem, dependendo do número de substituintes presentes no nitrogênio, amidas secundárias isto é amidas terciárias:
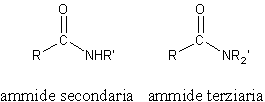
Nomenclatura amida
As amidas são chamadas pelo nome do ácido do qual são derivadas substituindo o sufixo -ico o sufixo -amida.
Para amidas secundárias e terciárias, os grupos de nitrogênio são precedidos pela letra N. Alguns exemplos:
Metanamida (formamida):
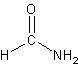
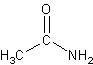
Etanamida (acetamida):
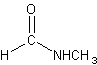
N-metilmetanamida (N-metilformamida):
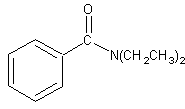
N, N-dietilbenzamida:
Propriedades gerais
Amidas são compostos que formam facilmente ligações de hidrogênio:
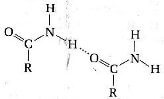
Por esse motivo, apresentam inesperadamente altos pontos de ebulição e fusão em relação à sua massa molecular. Grupos alquil ligados a nitrogênio tendem a diminuir a possibilidade de formar ligações de hidrogênio e a diminuir o ponto de ebulição e o ponto de fusão da amida.
Preparação das amidas.
As amidas podem ser obtidas de várias maneiras:
– Pela reação amina (RdoisNH) e ésteres (R’COOR ”).
Uma molécula de álcool (R”OH) também se desenvolve a partir da reação:
RdoisNH + R’COOR ” → R’CONRdois + R”OH
– Pela reação amina (RdoisNH) e cloretos de acila (R’COCl) com formação de cloreto de alquilamina (RdoisN.Hdois+ Cl–):
2 RdoisNH + R’COCl → R’CONRdois + RdoisN.Hdois+ Cl–
– Por reação de aminas com anidridos (R’COOCOR ”) com formação de alquilamino carboxilato (RdoisN.Hdois+ R”COO–):
2 RdoisNH + R’COOCOR ” → R’CONRdois + RdoisN.Hdois+ R”COO–
Nestas duas últimas reações, são necessários dois equivalentes de amina.
– Por reação entre aminas e ácidos carboxílicos..
O processo ocorre em duas etapas: na primeira, um aminocarboxilato (R ” é formadodoisNH2+RCOO–) que quando aquecido se decompõe para dar uma amida:
R ‘doisNH + RCOOH → R ”doisNH2+RCOO– → RCONR ‘dois + HdoisOU
Hidrólise de amidas.
Por hidrólise das amidas, os ácidos carboxílicos são obtidos:
RCONHdois + HdoisO → RCOOH + NH3
A reação é geralmente realizada por aquecimento prolongado e na presença de catalisadores ácidos ou básicos.
Redução de amida
Ao usar o hidreto de alumínio e lítio, é possível reduzir as amidas a aminas.
Exercícios sobre a nomenclatura da amida.
Se estiver interessado, você pode encontrá-los aqui: exercícios de nomeação de amidas.
Estude conosco
[ad_2]
Source link
