cicloalcanos
[ad_1]
Visão geral, propriedades e análise conformacional de cicloalcanos.
Cicloalcanos, também chamados naftenos ou cicloparafinas., são hidrocarbonetos cíclicos que têm a fórmula geral CnorteH2n (idêntico ao dos alcenos dos quais são isômeros estruturais) em que n = 1, 2, 3 etc.
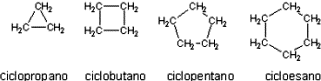
As estruturas e nomes dos quatro primeiros cicloalcanos são os seguintes:
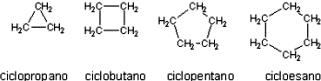
Anéis contendo 5 a 7 átomos de carbono são definidos. anéis comuns, enquanto aqueles com 3 ou 4 átomos são definidos pequenos ciclos, aqueles com 8-10 átomos de carbono ciclos médios e finalmente aqueles com 12 ou mais átomos são chamados macrociclos ou loops largos.
Ciclos e macrociclos comuns são semelhantes aos hidrocarbonetos acíclicos na maioria das propriedades físicas e químicas, enquanto ciclos pequenos e médios mostram propriedades bastante diferentes. As características incomuns dos anéis pequenos derivam do fato de que o sp3 eles tendem a ter ângulos de ligação próximos ao valor tetraédrico (109,5 °), enquanto as geometrias necessárias dos anéis pequenos reduzem esses ângulos para valores mais baixos.
Conformação de cicloalcano.
ciclopropano
a ciclopropano, que é composto por apenas três átomos de carbono, é necessariamente plano (uma vez que três pontos determinam um plano). O ângulo de ligação C – C – C é de apenas 60 °, muito menor que o ângulo tetraédrico comum (109,5 °) correspondente à hibridação sp3. Devido ao estresse causado principalmente pela pequena amplitude dos cantos, o ciclopropano possui um conteúdo energético muito alto e, portanto, é altamente reativo.
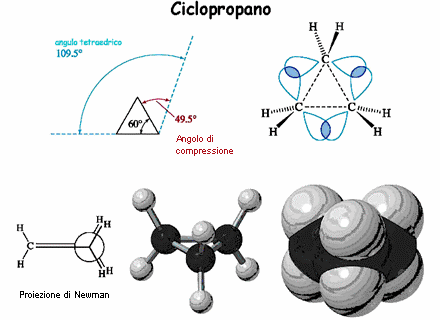
Os átomos de hidrogênio estão localizados acima e abaixo do plano da molécula e são ofuscados.
ciclobutano
a ciclobutano Não é plano, mas está disposto no espaço de acordo com a figura a seguir:
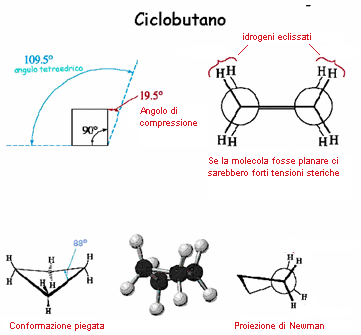
A estrutura angular do anel força os ângulos internos C – C – C a um valor mais baixo do que teria sido se a molécula fosse plana (90 °), mas o eclipse mais baixo dos átomos de hidrogênio compensa o estresse mais alto. angular.
ciclopentano
a ciclopentano Tem uma estrutura dobrada pelo mesmo motivo que é observado para o ciclobutano.
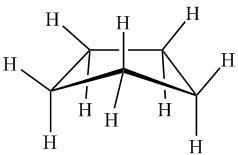
No ciclopentano, um átomo de carbono está fora do plano contendo os outros quatro átomos de carbono, mas o átomo de carbono fora do plano muda constantemente; de fato, um átomo do avião tenta entrar novamente, afastando o que segue. Portanto, a não planaridade gira em torno do ringue. Esse fenômeno é conhecido como pseudo rotação e é o mesmo fenômeno subjacente à forma flexível de ciclo-hexano.
Ciclohexano
O estudo da estrutura do ciclohexano é particularmente interessante devido ao seu alto grau de simetria. O ciclohexano, de fato, é um conformação chamada cadeira, onde os ângulos de ligação do CCC têm o valor ideal de um tetraedro perfeito (109,5 °). Nesta conformação, podemos ter dois tipos de átomos de hidrogênio: axial e equatorial. Dos hidrogênios axiais, três estão acima e três abaixo do plano mediano da molécula; Os hidrogênios equatoriais, por outro lado, estão aproximadamente nesse plano.
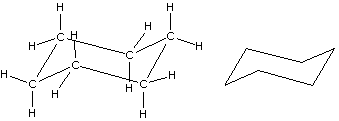
Na estrutura de sela do ciclo-hexano, é possível derrubar o anel: uma conformação da sela pode ser transformada em outra conformação da sela na qual os átomos de hidrogênio se tornaram equatoriais e vice-versa.
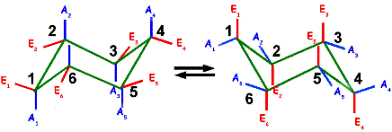
Essa inversão é muito rápida, mesmo em temperatura ambiente, enquanto desacelera a baixas temperaturas.
Para mais detalhes, consulte: análise conformacional do ciclo-hexano.
cicloheptano
A energia de torção de cicloheptano É principalmente devido a ângulos de torção desfavoráveis; de fato, não é possível ter matrizes perfeitamente escalonadas em torno de cada ligação C-C como no ciclo-hexano.
Ciclooctano e ciclone nano
a ciclooctano e ele ciclononano Eles também contêm considerável estresse torcional. Além disso, existem fortes repulsões transanulares hidrogênio-hidrogênio nesses anéis, devido ao fato de que os hidrogênios nas partes opostas do anel são mantidos próximos ao ponto de serem capazes de sofrer interações de Van der Waals.
Cyclodecano
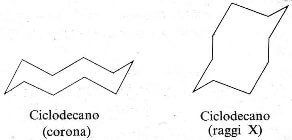
a ciclodecano Tem uma forma muito incomum. Se a molécula tivesse uma conformação da coroa, haveria tensões torcionais severas; Em vez disso, adotando a conformação indicada, a molécula diminui esse tipo de tensão, à custa da tensão angular. Os ângulos de ligação C – C – C no ciclodecano são consideravelmente maiores que o normal, com média de 117 °. Esses ângulos mais amplos permitem que a molécula se expanda e, portanto, reduzem a repulsão transanular de hidrogênio no anel.
Alguns tipos de cicloalcanos, adequadamente substituídos, podem dar isomerismo cis-trans.
Estude conosco
[ad_2]
Source link
