alcano
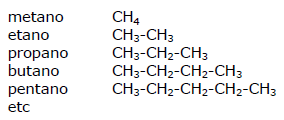
[ad_1]
Generalidades e propriedades dos alcanos.
Os alcanos são hidrocarbonetos que usam apenas ligações simples (ligações do tipo sigma).
A fórmula geral dos alcanos é CnorteH2n + 2, em que n = 1, 2, 3, 4 etc. Portanto:
para n = 1 CH4 4 (metanfetaminaano)
para n = 2 CdoisH6 6 (etano)
para n = 3 C3H8 (shore upano)
para n = 4 C4 4H10 (masano)
para n = 5 C5 5H12 (bloqueadoano)
etc.
OU:
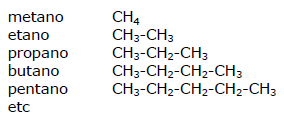
Para mais detalhes, consulte nomenclatura de alcanos.
Os alcanos também são chamados de hidrocarbonetos saturados. porque, para um determinado número de átomos de carbono, eles contêm o máximo possível de átomos de hidrogênio.
O carbono em alcanos sempre tem uma hibridação sp3 e apenas ligações simples estão presentes; portanto, a configuração dessa classe de compostos é tetraédrica.
No metano, por exemplo, existem ligações 4 sigma (σ), nascidas da superposição dos 4 orbitais híbridos sp3 carbono com 4 orbitais de hidrogênio do tipo s.
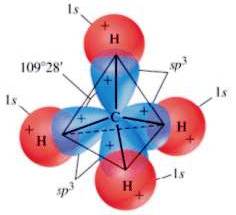
Estrutura de metano
Isomerismo alcano
Os alcanos, como muitos outros compostos orgânicos, podem dar isômeros de estrutura também chamados isômeros estruturais ou isômeros de cadeia.
Para os três primeiros termos de alcanos, não há problemas desse tipo, mas com butano foram isolados dois compostos que correspondem à mesma fórmula bruta (C4 4H10), mas eles têm propriedades físicas diferentes.
Estes são os norte-butano e isobutano:
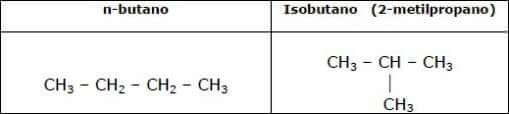
Estrutura do isômero de butano: a estrutura linear é definida como “normal”, enquanto a estrutura na qual um metil é anexado ao segundo átomo C na cadeia linear é definida como “iso”.
Conforme indicado na tabela a seguir, à medida que o número de átomos de carbono aumenta, o número de possíveis isômeros também aumenta:

Propriedades físicas
Os alcanos de cadeia linear do metano ao butano são gasosos e inodoro, do pentano ao pentadecano (Cquinze) são líquidos e o restante é sólido e inodoro.
As características físicas (ponto de ebulição, ponto de fusão, densidade e viscosidade) dessa classe homóloga variam com o peso molecular. Os isômeros lineares fervem em temperaturas mais altas que os ramificados. Assim, por exemplo, o n-butano, visto acima, ferve a uma temperatura mais alta que o isobutano.
Os alcanos são substâncias não polares e, portanto, insolúveis em água, mas são bons solventes para muitas substâncias orgânicas não polares. Eles têm um leve mas característico odor a gasolina. Eles têm uma densidade máxima de 0,8 g / ml e flutuam na água.
Forças atrativas fracas conhecidas como forças de Londres são exercidas entre moléculas não polares (como os alcanos). A intensidade dessas forças aumenta à medida que as dimensões moleculares aumentam: é por essa razão que o estado físico dos alcanos muda gradualmente, com o aumento do número de átomos de C, de gasoso para líquido e finalmente sólido.
Exercícios com alcanos
Você pode encontrá-los no seguinte link: exercícios sobre alcanos.
Pode ser interessante para você
Se você estiver interessado em um software que permita desenhar moléculas, vá para a próxima página: como usar o ChemSketch.
Estude conosco
[ad_2]
Source link
