Experiência Torricelli
[
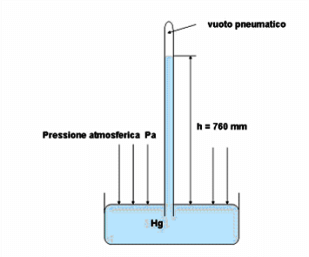
Experiência de Torricelli e cálculo da pressão atmosférica
físico e matemático italiano Evangelista Torricellidiscípulo de Galileu Galilei, em um conhecido experimentar em 1644 foi o primeiro a medir a pressão atmosférica ao nível do mar, conseguindo assim resolver a difícil questão de por que as bombas não funcionavam além do limite de altura de 10,7 metros.
Ele descobriu que este valor corresponde à pressão exercida (a uma temperatura de 0°C) por uma coluna de mercúrio de 760 mm de altura na superfície de 1 cmdois (centímetro quadrado).
Experiência Torricelli
Vamos ver em detalhes o que é o experimento torricelli.
Evangelista Torricelli, depois de encher um tubo longo e fino fechado em uma de suas duas extremidades com mercúrio, mergulhou a extremidade livre do tubo em um recipiente cheio de mercúrio.
Ele notou que, ao contrário do que ele esperava, o cano não esvaziava completamente, exceto ao nível do mar e a uma temperatura de 0°C. a coluna de mercúrio no tubo foi mantida a uma altura de 760 mm.
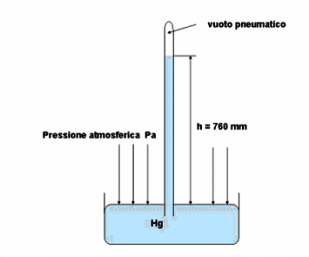
Representação do experimento Torricelli: a possibilidade de medir a pressão atmosférica tem sido de fundamental importância nas ciências meteorológicas.
De fato, a essa altura, a coluna de mercúrio exerce uma pressão igual à pressão atmosférica do ar que atua sobre o mercúrio.
O nível atingido pelo mercúrio fornece uma medida do valor da pressão atmosférica; este valor é bastante alto e corresponde aproximadamente à pressão exercida por uma massa de 2,1 kg agindo sobre uma moeda de um centavo.
No entanto, essa pressão não é sentida pelo homem, pois é compensada por uma pressão igual e oposta exercida pela atmosfera de dentro para fora do nosso corpo.
O experimento de Torricelli em breve
Vamos resumir brevemente o que Torricelli fez em seu famoso experimento: ele pegou um tubo de vidro fino de 1 m de comprimento, fechado em uma extremidade e preenchido com mercúrio; mantendo a outra extremidade fechada, Torricelli mergulhou o tubo em uma bandeja cheia de mercúrio e notou que o nível de mercúrio no tubo havia caído para uma altura de 760 mm da superfície da bandeja.
Isso significava que a pressão do ar sobre o mercúrio no copo suportava o peso do mercúrio na coluna. Torricelli também observou que o nível de mercúrio no tubo variava imperceptivelmente com a variação da pressão externa.
Cálculo da pressão atmosférica em Pascal
Se você quiser determinar a quantos Pascals corresponde a pressão atmosférica, basta fazer algumas considerações simples.
O peso da coluna de mercúrio (FP) que está dentro do tubo é igual a:
F.P = metro grama
mas a massa m de mercúrio é igual a:
m = dHg V (fórmula para calcular a massa)
no qual:
DHg = densidade do mercúrio = 1,36 104 kg/m3
V = volume de mercúrio contido no tubo de vidro
Mas:
V = Sh
no qual:
S = superfície do tubo
h = altura da coluna
Portanto:
F.P = metro grama = dHg V grama = dHg s h g
A pressão é dada pela relação entre a força do peso e a superfície, portanto:
P = FP /s=dHg S h g / S = dHg Hg
Portanto:
p = 1,36 104 kg/m3 0,760 m 9,81 N/kg = 1,01 105 Pensilvânia
Portanto, o valor de 1,01 · 10 é atribuído à pressão atmosférica5 Pensilvânia.
O que aconteceria se a água fosse usada em vez de mercúrio no experimento de Torricelli?
sim realizou o experimento de Torricelli usando água (DH2O = 1,00 103 kg/m3) em vez de mercúrio, para equilibrar a pressão atmosférica precisaríamos de uma coluna de água de 10,29 metros de altura.
Claro:
P = dhH2O G = 1,01105 Pensilvânia
Do qual:
hH2O = 1,01 105 / (dg) = 1,01 105 / (1,00 103 9,81) = 10,29 metros
Exercício 1
Você chega a um lugar nas altas montanhas onde a pressão atmosférica é 10% menor que a pressão atmosférica ao nível do mar.
Sob tais condições, qual seria a altura da coluna de mercúrio usada no experimento de Torricelli?
Você pode encontrar o exercício aqui: altura da coluna de mercúrio nas altas montanhas.
Exercício 2
Se no experimento de Torricelli tivesse sido usado ácido sulfúrico em vez de mercúrio (densidade = 1834 kg/m3) Qual seria a altura da coluna para poder medir a pressão atmosférica?
Você pode encontrar o procedimento aqui: barômetro de ácido sulfúrico.
Links Relacionados:
estude conosco