O que você sabe sobre notação atômica?

[ad_1]
Quando uma maçã é cortada em pedaços, definitivamente haverá momentos em que as fatias de maçã ficarão tão pequenas que não poderão mais ser cortadas, certo? Bem, a mesma coisa acontece quando dividimos os elementos. O elemento será dividido em milhões de partículas atômicas invisíveis.
A natureza de um elemento pode ser conhecida se conhecermos a natureza dos átomos que o compõem. Como os átomos não podiam ser observados usando os cinco sentidos, os químicos os explicaram usando símbolos na forma de números ou letras. Isso é o que geralmente chamamos de notação atômica. O que é isso?
A notação atômica pode ser interpretada como um conjunto ou sistema de símbolos (sinais) que descrevem o número do átomo, incluindo o número atômico (Z) que indica o número de prótons ou elétrons e o número de massa (A) que indica o número de prótons mais nêutrons no átomo.
Número Atômico (Z)
Esta parte da notação atômica descreve o número de prótons em um átomo. Este número atômico é uma característica de um elemento, porque o átomo é neutro, então o número de prótons é igual ao número de elétrons. Portanto, o número atômico também mostra o número de elétrons.
Esses elétrons acabarão por determinar as propriedades de um elemento. O número atômico é escrito ligeiramente para baixo antes dos símbolos do elemento. Como um exemplo, 8O, significando que o átomo de oxigênio tem um número atômico 8. Então, no núcleo atômico de O há 8 prótons e na camada atômica há 8 elétrons.
(Leia também: O que é notação científica?)
No entanto, os átomos também liberam ou aceitam elétrons sem alterar o elemento. O átomo que libera elétrons se transforma em íons negativos.
Exemplo: Enxofre (enxofre) tem um número atômico de 16, o que significa que o átomo S tem 16 prótons e 16 elétrons. Ion S4- tem 16 prótons e 12 elétrons, enquanto os íons S2- tem 16 prótons e 18 elétrons.
Número de massa (A)
A massa do elétron de um átomo é tão pequena que chega a ser considerada zero, de modo que a massa atômica é determinada pelo núcleo atômico, ou seja, os prótons e nêutrons. Os prótons e elétrons de um elemento são representados como números de massa que recebem o símbolo A para que possa ser escrito:
Número de massa (A) = número de prótons + número de nêutrons
ou
Número de nêutrons = Número de massa – Número atômico
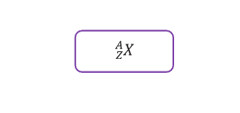
Na escrita, um único átomo é frequentemente equipado com um número atômico na parte inferior esquerda e um número de massa na parte superior esquerda e o símbolo para esse átomo é chamado de nuclídeo. Em geral, a notação de escrita de nuclídeos é a seguinte:
onde X = símbolo atômico, Z = número atômico e A = número de massa.
Se o átomo for neutro / sem carga, então prótons = nêutrons. O número de massa difere da massa atômica. O número da massa é sempre um número do mês e sem unidades, enquanto a massa atômica é um número que expressa a massa de 1 (um) átomo que geralmente é expressa em unidades de um (unidade de massa atômica).
[ad_2]
Source link