O princípio Aufbau: definição, regras e exceções
[ad_1]
O princípio de Aufbau, simplesmente, significa que os elétrons são adicionados aos orbitais assim como os prótons são adicionados a um átomo. O termo vem da palavra alemã “aufbau”, que significa “construir” ou “construção”. Os orbitais de elétrons mais baixos preenchem antes dos orbitais mais altos, “construindo” a camada de elétrons. O resultado final é que o átomo, íon ou molécula forma a configuração eletrônica mais estável.
O princípio de Aufbau descreve as regras usadas para determinar como os elétrons são organizados em camadas e subcamadas ao redor do núcleo atômico.
- Os elétrons vão para a subcamada com a menor energia possível.
- Um orbital pode conter no máximo 2 elétrons obedecendo ao princípio de exclusão de Pauli.
- Os elétrons obedecem à regra de Hund, que afirma que os elétrons se espalham antes do emparelhamento se houver dois ou mais orbitais energeticamente equivalentes (por exemplo, p, d).
Exceções ao princípio Aufbau
Como a maioria das regras, existem exceções. As subcamadas d e f semipreenchidas e totalmente preenchidas adicionam estabilidade aos átomos, de modo que os elementos do bloco d e f nem sempre seguem o princípio. Por exemplo, a configuração Aufbau prevista para Cr é 4sdois3d4mas a configuração observada é na verdade 4s13d5. Na verdade, isso reduz a repulsão elétron-elétron no átomo, uma vez que cada elétron tem seu próprio assento na subcamada.
Definição da regra Aufbau
Um termo relacionado é a “Regra de Aufbau”, que afirma que o preenchimento de diferentes subcamadas de elétrons é feito em ordem crescente de energia seguindo a regra (n + 1).
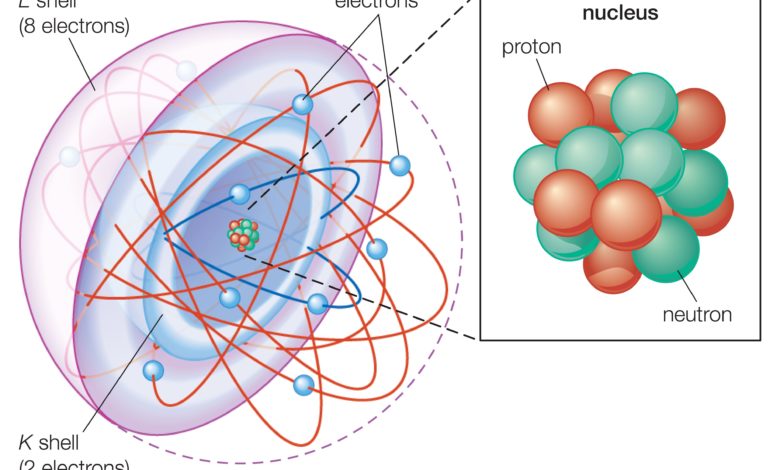
O modelo de casca nuclear é um modelo semelhante que prevê a configuração de prótons e nêutrons em um núcleo atômico.
[ad_2]
referências
